آموزش شیمی کنکور – نکات شعاع اتمی دوره ها در جدول تناوبی
دوستان عزیزم بارها بهتون گفتم که هیچ چیزی رو در شیمی نادیده نگیرین و یا سرسری نگاه نکنین. مخصوصا جدول ها و نمودارها رو با دقت بررسی کنید و نکات بسیار مهم کنکوری و طلایی را از آنها استخراج کنید.
در اینجا با یک مثال بهتون نشون میدم که چه جوری از نمودارها استفاده کنید. از این نموداری که میخوام براتون توضیح بدم در سال ۹۹ ازش سوال اومد ولی متاسفانه بسیاری از داوطلبین نتوانستند که جواب بدهند. در حالی که سوال بسیار آسانی بود و باید زیر ۵ ثانیه جواب می دادند…
شعاع اتمی دوره ها
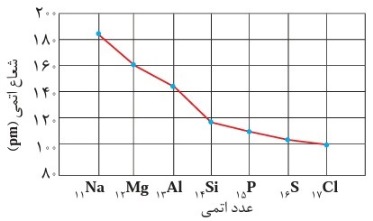
نمودار زیر روند تغییر شعاع اتمی عنصرها رو در دوره سوم جدول تناوبی نشان می دهد:
نکات بسیار مهم
۱- روند تغییر شعاع اتمی از چپ به راست کاهشی است.
۲- شعاع اتمی فلزات از شعاع تمی نافزات بزرگتر است.
۳- بزرگترین شعاع اتمی مربوط به فلزات قلیایی است.
۴- کوچکترین شعاع اتمی مربوط به هالوژن ها است.
۵- بیشترین اختلاف شعاع اتمی مربوط به فلزات قلیایی و هالوژن ها است.
۶- شیب تغییرات شعاع اتمی فلزات بزرگتر از شیب تغییرات شعاع اتمی نافلزات است.
توجه: دقیقا نکته ۶ در کنکور خارج از کشور سال ۹۹ آمده بود.
تدریس خصوصی و نیمه خصوصی شیمی دبیرستان و کنکور در تهران
 Iranian Chemist شیمیدان ایرانی
Iranian Chemist شیمیدان ایرانی



سلام اقای نباتی عزیز وقتتون بخیر ببخشید دلیل اینکه چرا شعاع اتمی آلومینیوم تا سیلیسیم بطور ناگهانی نسبت به بقیه تغییر زیادی کرده چیه؟ چرا شیب تغییرات نسبت به بقیه جدول بیشتره؟
مرسی از مطالب مفیدتون
سلام محمدجان. عزیزم این مبحث متاسفانه توی کتاب های شیمی دبیرستان نیست. ولی چون سوال پرسیدی جواب میدم تا اطلاعاتت تکمیل بشه.
عزیزم برای محاسبه شعاع اتمی و شعاع یونی فرمول های پیچیده ای هست ولی در همه این فرمول ها، شعاع با نسبت توان دوم شماره دوره بر عدد اتمی رابطه مستقیمی دارد. یعنی:
N2/Z
چون این عناصر همه متعلق به دوره سوم هستند پس N=3 بنابراین توان دومش نیز ۹ می شود. از طرفی در مخرج این رابطه باید عدد اتمی هر کدام از این عناصر گذشته شود. بنابراین برای عناصر دوره سوم خواهیم داشت:
سدیم ۰٫۸۱
منیزیم ۰٫۷۵
آلومینیوم ۰٫۶۹
سیلیسیوم ۰٫۶۴
فسفر ۰٫۶
گوگرد ۰٫۵۶
کلر ۰٫۵۳
حالا اگر دقت کنیم می بینیم که اختلاف این پارامتر بین هر دو عنصر متوالی به صورت زیر است:
سدیم-منیزیم ۰٫۰۶
منیزیم-آلومینیوم ۰٫۰۶
آلومینیوم-سیلیسیوم ۰٫۰۵
سیلیسیوم-فسفر ۰٫۰۴
فسفر-گوگرد ۰٫۰۴
گوگرد-کلر ۰٫۰۳
خب حالا اگر به این الگو دقت کنیم می بینیم که از آلومینیوم به بعد مقدار این اختلاف کاهش می یابد و هرچه به عناصر آخر دوره می رسیم باز هم این اختلاف کمتر و کمتر می شود.
به همین دلیل است که در عناصر اول دوره تغییرات شعاع زیاد است و در عناصر بعدی تغییرات شعاع کم است.
موفق باشی عزیزم
بسیار ممنونم استاد