ردیاب های زیستی
ویژگی های ردیاب زیستی
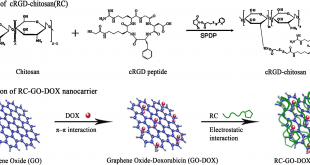
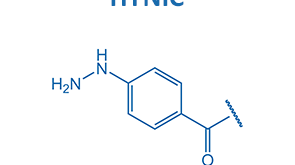
علاوه بر عوامل هدفمندی که تاکنون به منظور اتصال اختصاصی به رسپتورهاي سطح سلولهاي توموري مورد استفاده گرفته اند (پتيدها، آنتي باديها و قطعات ساختاری آن، افیبادیها، مولکولهای کوچک از قبیل ویتامین ها یا قندها)، امروزه دسته جدیدی از پروب های مولکولی به نام آپتامرها برای تشخیص تفاوت های مولکولی بیان شده در سطح غشاء سلول های نرمال و سرطانی شناسایی شده اند. پپتیدها، آنتی بادی ها و توالی های الیگونوکلئوتیدی به عنوان رادیوداروهای نسل سوم تکنیسیم بصورت مستقیم و یا به واسطه عوامل شلاتوری همچون ۲-مرکاپتو گلایسیل گلایسیل (MAG2)، مرکاپتو استیل تری گلایسین (MAG3)، هیدرازینو نیکوتینیک اسید (HYNIC)، Tricarbonyl و یا اتیلن دی سیستئین (EC) نشاندار می شوند. لازم به ذکر است که NHS-MAG3 و NHS-Hynic برای نشاندار سازی الیگومر ها با تکنیسیم m-99 بسیار مناسب می باشند. از مهمترین ویژگیها برای انتخاب ردیاب های هدفمند تومورهای سرطانی، اختصاصیت و میل ترکیبی مناسب اندازه و پایداری آن در بدن موجود زنده می باشد. علاوه بر این ها ویژگیهای دیگری از قبیل امکان تحریک سیستم ایمنی و قابلیت ورودشان به سلول نیز باید مورد توجه قرار گرفته شود. لازم به ذکر است که اندازه عامل هدفمند بر خصوصیات سنتیکی آنها موثر بوده و میتوان گفت که اندازه کوچک تر با نفوذ بهتر و سریعتر در تومور همراه خواهد بود اما جذب در بافتهای غیر توموری نیز با نسبتهای مختلف افزایش می یابد. همچنین اندازه عامل جستجوگر در مدت زمان حذف آن از بدن موجود زنده نیز بسیار موثر می باشد. در بحث درمان، اگر مدت ماندگاری در بدن موجود زنده بیشتر باشد مولکول ردیاب فرصت می یابد که مدت زمان بیشتری در معرض بافت هدف قرار گیرد و در نتیجه جذب توموری بالاتری را نتیجه می دهد. اما در کاربردهای تشخیصی، حذف سیستمی سریعتر نتایج مطلوب تری را به همراه دارد. بنابراین با توجه به آنکه در مقاصد تشخیصی، مسیر دفعی مطلوب دارو از طریق کلیهها می باشد حداکثر جرم مولکولی مناسب برای دفع از این مسیر KDa 70-60 بوده و این در حالی است که در ارتباط با مولکولهای بزرگتر دفع کبدی مسیر دفعی غالب می باشد. از سوی دیگر پایداری عوامل هدفمند نیز از جمله مباحث مهمی است که باید مد نظر قرار گیرد زیرا عوامل هدفمندی از قبیل پپتید ها و آپتامرها اگر بدون اعمال تغییراتی در ساختارشان که به منظور افزایش پایداری در آنها صورت می گیرد مورد استفاده قرار گیرند به سرعت توسط پپتیدازها و اگزونوکلئازهای سرمی خون تخریب میشوند. در ادامه بحث در رابطه باخصوصیات هر کدام از عوامل هدفمند ذکر شده توضیح مختصری ارائه و سپس مباحث مرتبط به آپتامرها شرح داده خواهد شد.
آنتی بادیها
آنتی بادیها به عنوان اولین عوامل هدفمند در دو دهه اخیر معرفی شدند که وزنی معادل kDa150 داشته و افینیتی بالایی به رسپتور یا آنتی ژن خاص خود در سطح سلول های سرطانی یا دیگر سلول ها نشان دادند. آن ها از اجزای مهم سیستم ایمنی بوده که در درمان تعدادی از بیماری ها از قبیل سرطان بسیار مورد توجه قرار گرفتند به گونه ای که استفاده از آنتی بادی های منوکلونال و یا فرگمنت های آن ها با مقاصد درمانی و تشخیصی در دهه های گذشته مورد توجه قرار گرفت و لیگاندهای دارویی هدفمندی از آن ها به عنوان دارو وارد بازار مصرف شد. اما نکته قابل توجه در ارتباط با آنتی بادیها، اندازه بزرگ آنهاست که سبب می شود کلیرانس خونی آنها بسیار آهسته صورت گیرد و همچنین نفوذشان را به تومور هایی که خونرسانی ضعیف دارند کاهش می دهد. بنابراین علی رغم اینکه این وضعیت برای مقاصد درمانی بسیار مفید است، استفاده از آنها را در کاربرد های تشخیصی محدود می سازد زیرا نسبت بالای جذب تومور به پس زمینه و حذف از بافتهای غیر هدف در زمان کم، از فاکتور موثر در کاربردهای تشخیصی است که مغایر با عملکرد آنتی بادیها است. از سوی دیگر ناحیه FC انتی بادی ها به سیستم رتیکواندوتلیال متصل شده و برداشت بالای رادیو نوکلوئید ها، دارو های سایتوتوکسیک یا توکسین های متصل شده به آنتی بادی ها را در مغز استخوان، کبد و طحال سبب شده و منجر به سمیت بالایی می شود.

پپتید ها
در مقایسه با آنتی بادیها، پپتید ها مولکول های کوچکتری ( معمولا کمتر از ۵۰ اسید آمینه) هستند و به همین دلیل خواص فارماکوکینتیک بهتری را از خود نشان می دهند. کلیرانس سریع از خون و بافت های غیر هدف و همچنین نفوذ بهتر آنها را به بافت هدف یا سلول های سرطانی نسبت به آنتی بادی ها از خواص مطلوب آنها به شمار می رود. تحریک کمتر سیستم ایمنی نیز از دیگر ویژگی های این دسته از عوامل هدفمند می باشد. همچنین این مولکول ها به راحتی سنتز شده و می توانند با رادیو نوکلوئید ها و یا توکسین ها برای اهداف درمانی و تشخیصی کانژوگه شوند. شناسایی توالی لیگاندهای پپتیدی به چند روش انجام میشود. مناسبترین روش استفاده از توالی پپتیدهای طبیعی با توانایی هدفمندی مد نظر است. تکنیک نمایش فاژ روش دیگری است که درآن ابراز پپتید ها برروی سطح باکتریوفاژ ها، یک فرصت برای شناسایی پپتیدهایی که تمایل باندینگ ویژه ای دارند را ایجاد می کند. پس از تشخیص توالی پپتید، سنتز آنها به سادگی انجام میشود و در نتیجه پیچیدگی کمتر ساختار، قابلیت بهینهسازی خصوصیات بیشتر است. تاکنون استفاده از پپتید ها در اشکال دارویی متنوع برای اهداف تشخیصی و بالینی گزارش شده است. از پرکاربردترین آنها می توان به آنالوگهای سوماتواستاتین، مشتقات بومبزین، RGD، مشتقات فیبرونکتین و … اشاره کرد.

مولکولهای کوچک
مولکولهای کوچک به عنوان دستهای جدید از عوامل هدفمند به دلیل قیمت مناسب، بسیار مورد توجه قرار گرفته اند. یکی از مولکولهای کوچک که به شکل گستردهای مورد بررسی قرار گرفته است اسید فولیک (فولات) است. فولات، ویتامین ۶B محلول در آب است که در رشد و تقسیم سلولی سریع بویژه در دوران جنینی نقش ضروری دارد. همچنین در سرطانها گیرندههای فولات در سطح سلولهای توموری بیان فوق العاده پیدا میکنند. با توجه به میل ترکیبی بالای فولات نسبت به گیرندههای آن (M 9-10 Kd =)، این مولکول قابلیت بالایی برای حمل ترکیبات درمانی و گزارشگر جهت تصویربرداری در سرطانها دارد. تاکنون به جز اسید فولیک، تعداد محدودی از مولکولهای کوچک دیگر با توانایی ردیابی تومورها معرفی شدهاند.

آپتامر
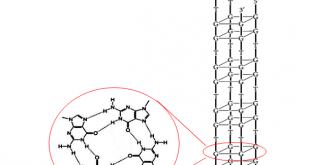
آپتامرها الیگونوکلئوتید تک رشتههای DNA، RNA یا پپتیدی هستند که گستره طول آنها از ۱۵ تا ۱۵۰ نوکلئوتید بوده و توالی بازهای تشکیل دهنده آنها تعیین کننده ساختار سه بعدی آنها می باشد. این ترکیبات می توانند با میل ترکیبی بالایی به اهداف اختصاصی خود متصل شوند. آپتامر ها برای محدوده وسیعی از اهداف از قبیل مولکول های کوچک، کربوهیدرات ها، پپتید ها یا پروتئین ها، نوکلئولیک اسیدها، لیپید ها و … انتخاب شده اند. مبحث آپتامرها در قسمت بعد با جزئیات بیشتر مورد بررسی قرار گرفته است.

نویسنده مقاله: خانم دکتر زهره نوع پرست متخصص داروسازی هسته ای
 Iranian Chemist شیمیدان ایرانی
Iranian Chemist شیمیدان ایرانی