آموزش آرایش الکترونی اتم کروم در کوتاهترین زمان
تدریس آرایش الکترونی عناصر استاد دکتر نباتی
دانش آموزان عزیزم مبحث آرایش الکترونی عناصر از فصل اول شیمی دهم دبیرستان جزو مباحث سوال خیز کنکور می باشد. اتم کروم جزو عناصری است که چندین بار در آزمون های کنکور سراسری مورد طرح سوال واقع شده است. دلیل تست خیز بودن آن هم به نکات پر شدن الکترون ها در زیرلایه های آن برمیگردد.
لذا امروز در این مقاله می خواهم به طور کامل آرایش الکترونی عنصر کروم و یون های آن را به شما عزیزانم آموزش دهم.
نحوه نوشتن آرایش الکترونی عنصر کروم
همچنان که در مقاله قبلی (از اینجا می توانید مطالعه کنید) نیز توضیح دادم، نحوه پر شدن زیرلایه های الکترونی عناصر از رابطه کنکوری زیر پیروی می کند:
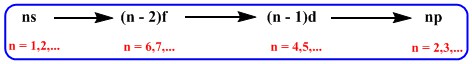
طبق این رابطه کنکوری، آرایش الکترونی برای عنصر کروم (Cr) با عدد اتمی ۲۴ به صورت زیر خواهد بود:
۱s2 2s2 2p6 3s2 3p6 4s2 3d4
اما توجه داشته باشید که طبق اصل پایداری ترازهای پر و نیمه پر، این آرایش الکترونی اشتباه است!!! (حالا فهمیدید که چرا طراحان کنکور همیشه دوست دارند از آرایش الکترونی این عنصر سوال طرح کنند؟؟!!! چون می دانند که بالای ۹۰ درصد داوطلبان آرایش الکترونی بالا را خواهند نوشت و در ادامه به سوالات جواب خواهند داد!!)
با توجه به اصل پایداری زیرلایه های الکترونی پر و نیمه پر، این آرایش الکترونی برای اینکه به پایداری بالایی برسد تمایل دارد که یک الکترون از ۴s2 کم شده و به ۳d4 اضافه شود تا هر دو به آرایش نیمه پر برسند:
۱s2 2s2 2p6 3s2 3p6 4s1 3d5
در قدم آخر، بعد از پر کردن زیرلایه ها از الکترون ها، زیرلایه ۳d پایداری بالایی یافته و پایینتر از زیرلایه ۴s قرار خواهد گرفت. بنابراین آرایش الکترونی نهایی عنصر کروم به صورت زیر می باشد:
۱s2 2s2 2p6 3s2 3p6 3d5 4s1
نحوه نوشتن آرایش الکترونی یون های کروم
موقع یونش، الکترون ها ابتدا از زیرلایه ۴s جدا می شوند و سپس از زیرلایه ۳d جدا خواهند شد.
برای مثال آرایش الکترونی یون +Cr به صورت زیر خواهد بود:
۱s2 2s2 2p6 3s2 3p6 3d5
آرایش الکترونی یون +Cr2 به این صورت خواهد بود:
۱s2 2s2 2p6 3s2 3p6 3d4
حالا اگر خوب یاد گرفتید به سوال کنکوری زیر خودتان جواب بدهید:
تست شیمی دهم کنکور سراسری
در یون +Cr3 چند الکترون در زیرلایه با عدد کوانتومی فرعی l = 2 قرار دارد؟
الف: ۳
ب: ۴
ج: ۵
د: ۶
موفق باشید

تدریس تحلیلی و تضمینی شیمی کنکور و المپیاد در تهران
 Iranian Chemist شیمیدان ایرانی
Iranian Chemist شیمیدان ایرانی



