تدریس المپیاد شیمی و شیمی کنکور
استاد شیمی آنلاین (همه شهرها) و حضوری (فقط تهران)
دکتر مهدی نباتی – مدرس شیمی رتبه های برتر ایران
المپیاد شیمی مرحله اول المپیاد شیمی مرحله دوم تدریس المپیاد شیمی مرحله اول تدریس المپیاد شیمی مرحله دوم تدریس خصوصی المپیاد شیمی مرحله اول
المپیاد شیمی مرحله اول المپیاد شیمی مرحله دوم تدریس المپیاد شیمی مرحله اول تدریس المپیاد شیمی مرحله دوم تدریس خصوصی المپیاد شیمی مرحله اول
تیپ سوال المپیاد شیمی مرحله دوم
با توجه به دو شرط زیر، چگالی (g/cm3) و APF% سلول واحد سزیم کلرید چقدر است؟ (شعاع یون های سزیم و کلرید به ترتیب برابر ۱۸۱ و ۱۶۷ پیکومتر می باشد. جرم اتمی سزیم و کلر نیز به ترتیب ۱۳۲٫۹ و ۳۵٫۵ گرم بر مول می باشد.)
* آنیون ها با هم مماس نیستند.
* آنیون ها با کاتیون ها مماس هستند.
المپیاد شیمی مرحله اول المپیاد شیمی مرحله دوم تدریس المپیاد شیمی مرحله اول تدریس المپیاد شیمی مرحله دوم تدریس خصوصی المپیاد شیمی مرحله اول
پاسخ:
دانش آموزان عزیزم با توجه به شکل زیر می بینیم که هر کاتیون سزیم ور وسط مکعب قرار گرفته و ۸ یون کلرید در ۸ گوشه مکعب جای گرفته اند. با توجه به اینکه هر یون کلرید (برای مثال یون کلریدی که با رنگ زرد مشخص شده است را دقت کنید) بین ۸ مکعب مشترک است، پس انگار یک هشتم هر یون کلرید متعلق به یک مکعب است و از آنجایی که ۸ گوشه داریم پس ۸ تا یک هشتم می شود یک یون کلرید. لذا در هر مکعب یک یون سزیم و یک یون کلرید داریم.
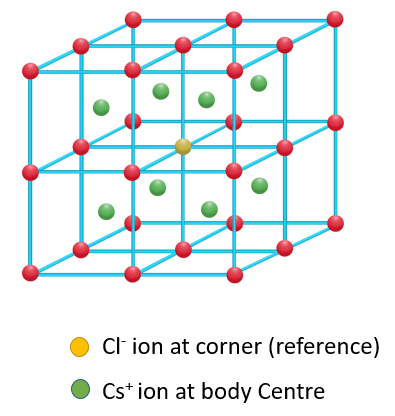
برای محاسبه چگالی بایستی حجم یک سلول واحد و جرم یک سزیم کلرید را حساب کنیم.
جرم سزیم کلرید را از طریق رابطه زیر می توانیم حساب کنیم:
m / M = N / NA
⇓
m / 168.4 = 1 / (6.022 × ۱۰۲۳)
⇓
m = 2.8 × ۱۰-۲۲ g
در این رابطه m و M و N و NA به ترتیب نشان دهنده جرم و جرم مولی و تعداد مولکول و عدد آووگادرو است.
المپیاد شیمی مرحله اول المپیاد شیمی مرحله دوم تدریس المپیاد شیمی مرحله اول تدریس المپیاد شیمی مرحله دوم تدریس خصوصی المپیاد شیمی مرحله اول
حالا باید حجم یک سلول واحد را حساب کنیم. از آنجایی که سلول واحد مکعبی است بنابراین حجم آن برابر مکعب یک ضلع یعنی a3 می باشد.
ولی چون ضلع را نداریم ابتدا باید ضلع (a) را حساب کنیم. از آنجایی که سوال گفته که آنیون ها و کاتیون ها به هم مماس هستند، بنابراین قطر مکعب، از مجموع قطر یک یون سزیم (دو برابر شعاع سزیم) و یک یون کلرید (دو برابر شعاع یون کلرید) تشکیل شده است:
۳ a2 = (2RCl- + 2RCs+)2
⇓
۳ a2 = ((2×۱۶۷) + (۲×۱۸۱))۲
⇓
a = 401.84 pm
محاسبه حجم مکعب:
V = a3
⇓
V = 401.842
⇓
V = 6.49 × ۱۰۷ pm3
المپیاد شیمی مرحله اول المپیاد شیمی مرحله دوم تدریس المپیاد شیمی مرحله اول تدریس المپیاد شیمی مرحله دوم تدریس خصوصی المپیاد شیمی مرحله اول
محاسبه چگالی سلول واحد سزیم کلرید:
ρ = m / V
⇓
ρ = (۲٫۸ × ۱۰-۲۲) / (۶٫۴۹ × ۱۰۷)
⇓
ρ = ۴٫۳۱ × ۱۰-۳۰ g/pm3
⇓
ρ = ۴٫۳۱ g/cm3
بنابراین، چگالی سلول واحد سزیم کلرید برابر با ۴٫۳۱ گرم بر سانتی متر مکعب است.
المپیاد شیمی مرحله اول المپیاد شیمی مرحله دوم تدریس المپیاد شیمی مرحله اول تدریس المپیاد شیمی مرحله دوم تدریس خصوصی المپیاد شیمی مرحله اول
درصد ضریب پکینگ اتمی %APF:
%APF یعنی درصدی از حجم یک سلول واحد مکعبی شکل که توسط یون ها اشغال شده است. بنابراین کافی است حجم سزیم کلرید را حساب کرده و تقسیم بر حجم کل مکعب بکنیم و ضرب در ۱۰۰ نماییم.
با توجه به اینکه یون ها کروی است، کافیه که حجم یون های سزیم و کلرید را حساب کنیم و با هم جمع بزنیم تا حجم سزیم کلرید به دست آید:
VCsCl = VCs+ + VCl- = (4πR3Cs+/3) + (۴πR3Cl-/3)
⇓
VCsCl = 4.433 × ۱۰۷ pm3
المپیاد شیمی دکتر نباتی
حالا می توانیم درصد APF را حساب کنیم:
APF% = [(4.433 × ۱۰۷) / (۶٫۴۹ × ۱۰۷)] × ۱۰۰
⇓
APF % = 68.3 %
بنابراین درصد ضریب چینش اتمی در سلول واحد شبکه کریستالی سزیم کلرید برابر با ۶۸٫۳ درصد می باشد.المپیاد شیمی مرحله اول المپیاد شیمی مرحله دوم تدریس المپیاد شیمی مرحله اول تدریس المپیاد شیمی مرحله دوم تدریس خصوصی المپیاد شیمی مرحله اول
*** در فایل ویدیویی زیر، روش محاسبه چگالی و درصد APF سلول واحد شبکه های کریستالی را به طور کامل برای شما عزیزان توضیح داده ام.
پس حتما فایل آموزشی زیر را به دقت ببینید و نکات و تکنیک های گفته شده برای حل مسائل پیچیده شبکه های کریستالی را یاد بگیرید.
المپیاد شیمی استاد نباتی
المپیاد شیمی استاد نباتی
روش تعیین چگالی و درصد APF سلول واحد شبکه های کریستالی
المپیاد شیمی استاد نباتی
المپیاد شیمی استاد نباتی
با آرزوی موفقیت برای شما دانش آموزان عزیزم
المپیاد شیمی استاد نباتی
استاد شیمی کنکور و المپیاد ایران
المپیاد شیمی استاد نباتی

المپیاد شیمی استاد نباتی
تدریس خصوصی آنلاین شیمی کنکور و المپیاد شیمی ایران
المپیاد شیمی استاد نباتی
 Iranian Chemist شیمیدان ایرانی
Iranian Chemist شیمیدان ایرانی


