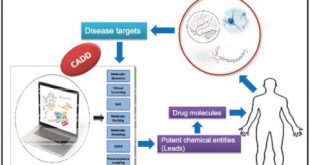
مکانیک کوانتومی توصیف ریاضی صحیح از رفتار الکترونها و در نهایت توصیف شیمی با استفاده از ریاضی است.
از دیدگاه نظری، مکانیک کوانتومی میتواند هر خاصیتی از یک اتم یا مولکول مجزا را به طور دقیق، فقط برای سیستمهای تک الکترونی حل شده اند. روشهای زیادی برای حل تقریبی سیستمهای چند الکترونی توسعه یافته اند. این تقریبها میتوانند بسیار مفید باشند؛ اما محقق باید بداند در چه شرایطی تقریب به کار رفته اعتبار دارد و صحت نتایج، به چه میزان مورد نیاز است.
دو فرمول بندی معادل در مکانیک کوانتومی به وسیله شرودینگر و هایزنبرگ ارائه شده است که اکثرا فقط از روش شرودینگر استفاده میشود.
با تعیین تابع موج در مکانیک کوانتومی، هر خاصیتی از یک مولکول منفرد قابل تعیین است. این کار با تعیین مقدار قابل انتظار عملگر آن خاصیت، <>، انجام میگیرد. اگر تابع موج استفاده شده دقیق باشد، مقدار انرژی همان مقدار انرژی است که از معادله شرودینگر به دست می آید، اما برای تابع موج تقریبی، فقط میتوان انرژی تقریب را محاسبه کرد. به این انرژی، انرژی تغییر (variational energy) میگویند، زیرا همواره مقدار آن از انرژی دقیق، بیشتر یا مساوی است. با قرار دادن عملگرهای مختلف در عبارت مقدار قابل انتظار میتوان خواص مشاهده پذیر مختلف را به دست آورد؛ مانند دوقطبی یا چگالی الکترونی. به جز انرژی، خواص دیگر تغییری نیستند؛ زیرا برای به دست آوردن تابع موج در روشهای شیمی محاسباتی، فقط از هامیلتونی استفاده میشود.
روش دیگر به دست آوردن خواص مولکولی، استفاده از نظریه هلمن-فینمن (Hellmann Feynman) است. این نظریه بیان میکند که مشتق انرژی نسبت به خاصیت P به صورت زیر تعریف میشود:

این رابطه اغلب برای محاسبه خواص الکتروستاتیک استفاده میشود. همه روشهای تقریبی از نظریه هلمن-فینمن تبعیت نمیکنند؛ بلکه فقط روشهای تغییری مانند HF، MCSCF، CI و CC از این نظریه تبعیت میکنند.
 Iranian Chemist شیمیدان ایرانی
Iranian Chemist شیمیدان ایرانی