مقایسه اثر شلاتور هایی از جنس اسیدآمینه با HYNIC
از میان تکنیکهای فراوان برای تصویربرداری آنکولوژی و بیماریهای عفونی، تکنیکهای پزشکی هسته ای از جمله SPECT و PET اهمیت زیادی دارند. این تکنیکها دارای حساسیت بالایی می باشند و بنابراین تنها مقدار کمی از مواد برای ایجاد یک تصویر مناسب لازم می باشد. اغلب مطالعات کلینیکالی از عاملهای تصویربرداری نشاندار شده با تکنسیم-۹۹m استفاده میکنند. تحقیقات اخیر بر روی کمپلکسهای کئوردینه کوچکی تمرکز کردند که در داخل بدن بر اساس بار، اندازه و هیدروفیلیسیته توزیع میشوند و به طور اختصاصی گیرنده خاصی را مورد هدف قرار می دهند. به منظور استفاده از این رادیو نوکلئوتیدها برای تصویر برداری به طریق روش SPECT و اتصال به پپتیدها و آنتی بادیها، از شلاتورهایی نظیر HYNIC, MAG3 و MAG2 و گروههایی از جنس اسید آمینهها به منظور تشکیل اتمهای دهنده N3S استفاده کردند. یکی از مزایای این شلاتورهای بر پایه پپتید، این میباشد که در هنگام سنتز پپتید هدفمند، این شلاتورها نیز به راحتی سنتز و در یک مرحله بطور اختصاصی به آنها اضافه میشوند. در مورد شلاتور HYNIC، الگوی توزیع بیولوژیکی، پایداری و لیپوفیلیسیته آن بستگی دارد به نوع کولیگاندی که در آن استفاده می شود. در اینجا ذکر مثالهایی از پپتیدها و آنتی بادیهایی که از طریق اضافه کردن توالی اسیدآمینه یا اسیدآمینههای موجود در ساختار اولیه خود پپتید یا آنتی بادی بدون تغییر دومین اتصالی به گیرنده مورد هدف، نشاندار شده اند برای تاکید بر علت استفاده این گروهها در این مطالعه ضروری است.
پپتید های P829 و p587 از جمله مشتقات پپتید سوماتوستاتین هستند. در حالیکه در ساختاراصلی p587 از اسید آمینه های دهنده مونو تیول-تری امید به منظور اتصال به تکنسیم-۹۹m استفاده میشود، در پپتید P829 از مونوتیول-مونو آمین-بیس آمید استفاده میشود. این امر باعث ایجاد بار منفی در کمپلکس بعد از نشاندارسازی در پپتید p587 و دفع بیشتر آن از طریق سیستم کبدی و ایجاد بار خنثی در پپتید P829 و خروج بیشتر آن از طریق سیستم کلیوی می شود.
به منظور نشاندار سازی پپتید Octreotide با تکنسیم-۹۹m، ۳ توالی ۴ پپتیدی acetyl-Gly-Gly-Cys-Gly، acetyl-Gly-Gly-Cys-Lys و acetyl-Ser-Ser-Cys-Gly را به این پپتید اضافه کردند. توزیع بیولوژیکی این ۳ پپتید نشان داد که سرعت خروج acetyl-Gly-Gly-Cys-Gly از خون از همه سریعتر میباشد و همچنین هیچ تجمع ویژهای در بافتهای غیر هدف در هر ۳ مورد دیده نشد.
پپتید UBI که یک عامل برای تصویربرداری عفونت میباشد در ساختار آن ۵ اسید آمینه آرژینین و یک اسید آمینه لیزین وجود دارد که به راحتی از طریق روش مستقیم با تکنسیم-۹۹m در pH های بالاتر از ۸ نشاندارسازی می شوند. اگر بخواهیم این نشاندارسازی را با زمانی که از شلاتور HYNIC استفاده می شود مقایسه کنیم، پپتید ۹۹mTc-UBI دارای خلوص رادیوشیمیایی بالاتر، کلیرانس سریعتر از کلیه است.
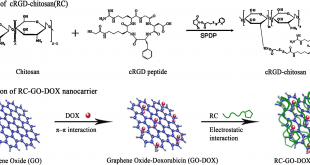
مشتقات حلقوی پپتید RGD برای گیرنده ανβ۳ به منظور مورد هدف قرار دادن رگزایی سلول های توموری استفاده می شوند. برای نشاندار سازی این ترکیب از توالی پپتیدی (Orn)3-CGG) که سری سیستئین-گلایسین-گلایسین آن به عنوان گروه شلات کننده تکنسیم-۹۹m میباشد استفاده کردند و ۳ تا اسید آمینه اورنیتین آن به منظور بهبود خواص توزیع زیستی و بیولوژیکی در ساختار آن بکار میرود. این پپتید نشاندارسازی پایدار، کلیرانس خونی سریع، دفع بیشتر از طریق سیستم کلیوی و نسبت تومور به زمینه بالاتری نسبت به دیگر عوامل شلات کننده از خود نشان داد.
برای مورد هدف قرار دادن گیرنده HER2 و تصویربرداری آن، نشاندارسازی افیبادی ZHER2.342 با تکنسیم-۹۹m به همراه گروههای پپتیدی مرکاپتو-گلایسین-Dسرین-گلایسین، مرکاپتو- گلایسین-سرین-گلایسین، مرکاپتو-سرین-سرین-سرین مورد مطالعه قرار دادند. برای این پپتیدها KD بین ۳۰۰-۴۰۰ پیکو مولار گزارش شد و بازده نشاندارسازی و پایداری در سرمmaSSS-ZHER2:342 از بقیه بیشتر بود. در بررسیهای توزیع زیستی، این ساختار دارای زمان پایداری بیشتر در تومور و پایداری کمتر در دیگر اندامها نسبت به توالی پپتیدی دیگر بود. همچنین کمترین دفع سیستم کبدی از طریق آن مشاهده شد.
در تحقیقات دیگر به منظور پیدا کردن بهترین توالی پپتیدی برای کمپلکس شدن با تکنسیم-۹۹m مربوط به نشاندارسازی ZHER2.342، خواص maCGGG-ZHER2:342را با ۹۹mTc-CGGG-ZHER2:342 و ۹۹mTc-CGG-ZHER2:342 که دارای اسید آمینه سیستئین هستند مقایسه کردند. نتایج نشان داد که توالی دارای سیستئین نسبت به مرکاپتو، ۳ برابر کاهش در حذف سیستم کبدی داشتند و همچنین سرعت خروج آنها از سیستم کلیوی بیشتر گزارش شد. بطور خلاصه افی بادی حاوی شلاتورهای سیستئینی بطور پایدارتری با تکنسیم-۹۹m کمپلکس میدهند، به سرعت از خون حذف میشوند و تجمع آنها در تومور قابل توجه میباشد.
از میان ۴ توالی پپتیدی GGGC، GGSC، GGEC، GGKC که به افیبادی ZHER2 برای نشاندار سازی تکنسیم-۹۹m متصل میشوند، بیشترین KD برای GGEC محاسبه شده است که برابر است با ۲۵۵ پیکو مولار و کمترین آن نیز برای GGGC محاسبه شده است. دو توالی GGKCو GGEC قویترین زمان بازماندگی در سلول توموری و بیشترین تجمع در سیستم کبدی را داشتند. کمترین مقدار داخل شدن به سلول مربوط به GGGC و کمترین سطح اکتیویته در کلیه نیز مربوط به همین پپتید می باشد.
نویسنده مقاله: خانم دکتر حمیده صباح نو متخصص داروسازی هسته ای
 Iranian Chemist شیمیدان ایرانی
Iranian Chemist شیمیدان ایرانی