نکات کنکوری شیمی دبیرستان – سالیسیلیک اسید
دوستان عزیز، متاسفانه خیلی از مباحث شیمی در کتاب های درسی به صورت گذرا فقط اشاره شده است. از آن طرف هم بسیاری از دبیران و مدرسان فقط به صورت حفظی مطالب را یاد دانش آموزان می دهند. در حالی که سوالات کنکور امسال نشان داد که دیگر خبری از سوالات حفظی و فرمولی نخواهد بود و سوالات به سمت و سوی تحلیلی پیش رفته اند.
لذا شما دانش آموزان باید روش تحلیل مباحث شیمی را یاد بگیرید. ممکن است یک مطلب فقط به صورت یک اسم در کتاب به آن اشاره شده باشد ولی شما باید تمامی نکات احتمالی آن مبحث را استخراج کنید تا بتوانید به سوالات تحلیلی کنکور جواب دهید.
یکی از این موارد، ترکیب سالیسیلیک اسید است که در کتاب فقط اشاره مختصری به آن شده است. با ما همراه باشید تا ببینید که از یک ترکیب شیمیایی چقدر مطالب و نکات طلایی می توان استخراج کرد که از هر کدام می توان سوال در کنکور طرح کرد.
ترکیب سالیسیلیک اسید
خوب به ساختار سالیسیلیک اسید توجه کنید:
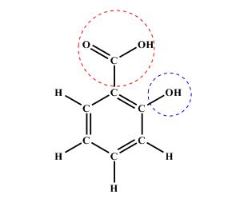
نکات طلایی سالیسیلیک اسید
۱- یک حلقه بنزن و دو گروه عاملی (گروه هیدروکسیل و گروه کربوکسیلیک اسید) دارد.
۲- یک ترکیب آلی است.
۳- یک ترکیب آروماتیک است (چون در ساختار خود حلقه بنزن دارد).
۴- فرمول مولکولی آن C7H6O3 است.
۵- جرم مولکولی آن ۱۳۸ می باشد.
۶- جمعا ۲۰ پیوند دارد.
۷- جمعا ۴۰ الکترون پیوندی دارد.
۸- جمعا ۱۲ پیوند یگانه دارد.
۹- جمعا ۴ پیوند دوگانه دارد.
۱۰- مولکول قطبی است.
۱۱- توانایی تشکیل پیوند هیدروژنی با مولکول دیگر سالیسلیک اسید دارد.
۱۲- توانایی تشکیل پیوند هیدروژنی درون مولکولی دارد. یعنی گروه های عاملی هیدروکسیل و کربوکسیلیک اسید درون خود مولکول با هم پیوند هیدروژنی می دهند. ۳ نوع پیوند هیدروژنی درون مولکولی می تواند تشکیل دهد.
۱۳- جمعا ۶ جفت الکترون ناپیوندی دارد (هر اکسیژن ۲ جفت الکترون ناپیوندی دارد).
۱۴- جمعا ۱۲ الکترون ناپیوندی دارد (هر جفت الکترون ناپیوندی برابر با ۲ الکترون ناپیوندی است).
۱۵- با آسپرین فقط در گروه عاملی هیدروکسیل مشابهت دارد.
۱۶- با متیل سالیسیلات فقط در گروه عاملی هیدروکسیل مشابهت دارد.
۱۷- ترکیب پایداری است.
۱۸- حلقه بنزن آن با برم واکنش نمی دهد. چون فقط باند دوگانه های مجزا مثل اتیلن (اتن) با برم جواب می دهد.
۱۹- جامد است.
۲۰- اسید آلی است.
۲۱- سفید رنگ است.
۲۲- نکته بسیار بسیار مهم: در آب حلالیت بسیار کمی دارد با آنکه ترکیبی کاملا قطبی است. دلیل آن این است که گروه های عاملی آن پیوند هیدروژنی درون مولکولی داده و به عبارتی با خودشان درگیر هستند و بنابراین فرصت نمی کنند که بتوانند با مولکول های آب پیوند هیدروژنی زیادی تشکیل دهند به همین خاطر اگر چه قطبی است ولی حلالیت کمی در آب دارد.
تدریس خصوصی و گروهی شیمی دبیرستان و کنکور در تهران
 Iranian Chemist شیمیدان ایرانی
Iranian Chemist شیمیدان ایرانی




