آموزش نکات کنکوری و المپیادی شیمی دبیرستان
دانش آموزان عزیزم تقریبا یکی از سوالاتی که هر سال در کنکور سراسری می آید مربوط به آبکافت (هیدرولیز) پلیمرها است. در این مقاله می خواهم یک روش و تکنیک کنکوری به شما آموزش بدهم که خیلی راحت به چنین سوالاتی جواب بدهید.
برای اینکه این تکنیک را بهتون یاد بدم به این سوال کنکور توجه کنید:
تست شیمی کنکور سراسری
اختلاف جرم منومرهای سازنده پلی استر با واحد تکرار شونده زیر چقدر است؟
(C = 12 و H = 1 و O = 16)
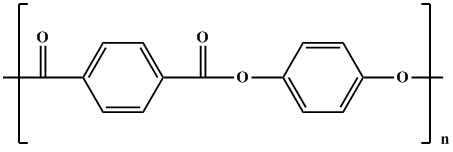
الف: ۶۰
ب: ۵۸
ج: ۵۶
د: ۵۴
پاسخ:
دانش آموزان عزیزم هر موقع چنین سوالی دیدید که در مورد منومرهای سازنده یک پلی استر مطرح شده بود و یا حرف از آبکافت زده بود، خیلی سریع تکنیک طلایی زیر را به کار بگیرید:
تکنیک طلایی: به گروه های کربونیل، هیدروکسی اضافه کنید و به اتم های اکسیژن، هیدروژن اضافه کنید.
با این تکنیک خیلی راحت به منومرهای سازنده پلی استر می رسیم.
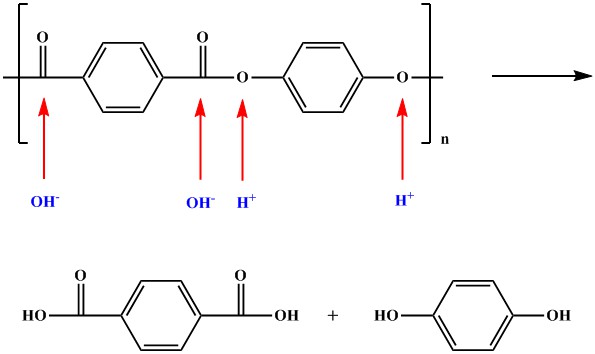
خب الان برسیم درخواست سوال کنکور که از ما اختلاف جرم منومرهای سازنده را خواسته است. برای پاسخ به این خواسته، دو راه حل داریم.
راه حل اول: اینکه جرم مولکولی هر کدام از منومرها را حساب کنیم و سپس جرم مولکولی ها را از هم کم کنیم:
۱۶۶ = ۱ × ۶ + ۱۶ × ۴ + ۱۲ × ۸ = جرم مولکولی دی اسید
۱۱۰ = ۱ × ۶ + ۱۶ × ۲ + ۱۲ × ۶ = جرم مولکولی دی اُل
۵۶ = ۱۱۰ – ۱۶۶ = اختلاف جرم منومرها
راه حل دوم: با این تکنیک کنکوری خیلی سریع به جواب می رسید و دیگر نیازی به محاسبات ندارد (یادتان باشد که در امتحان مدرسه بایستی از روش اول استفاده کنید چون روش دوم روش کنکوری است).
در این روش نیازی نیست که جرم مولکولی تک تک منومرها را حساب کنیم و سپس از همدیگر کم کنیم.
در این روش کافی است که قسمت های یکسان مولکول ها (که در اینجا در حلقه های بنزنی و گروه های هیدروکسیل مشترک هستند) را حذف کنیم و فقط جرم قسمت های باقیمانده را حساب کنیم و از همدیگر کم کنیم.
با دقت به ساختار مولکول ها می بینیم که ترکیب دی اسید، فقط دو گروه کربونیل C=O نسبت به ترکیب الکلی اضافه تر دارد. بنابراین:
۲۸ = ۱۶ + ۱۲ = جرم یک گروه کربونیل
۵۶ = ۲۸ × ۲ = جرم دو گروه کربونیل
گزینه صحیح:
با استفاده از تکنیک های طلایی آموزش داده شده، دیدیم که گزینه ج جواب صحیح این سوال کنکور سراسری می باشد.

تدریس خصوصی و گروهی شیمی دهم و یازدهم و دوازدهم در تهران
 Iranian Chemist شیمیدان ایرانی
Iranian Chemist شیمیدان ایرانی



