آموزش نکات کنکوری ساختار مولکولی ویتامین C
دانش آموزان عزیزم، یکی از مهم ترین و سوال خیزترین قسمت های شیمی در سوالات کنکور سال های اخیر مربوط به شکل ها و مولکول ها بوده است. در کتاب های درسی یا فقط اسم یک ترکیب شیمیایی آمده یا فقط یک شکل یا یک نمودار آورده اند و هیچ توضیحی در مورد آن نداده اند. به همین خاطر بایستی شدیدا به روی این موارد تمرکز کنید و تمامی اطلاعات را از آن بیرون بکشید.
ما در این مقاله می خواهیم نگاه دقیق تری به ساختار شیمیایی ویتامین سی (C) بیاندازیم.
نکات کنکوری و مهم ویتامین سی
لطفا به ساختار مولکولی ویتامین C توجه کنید (حتما ساختار مولکولی اش را یاد بگیرید):
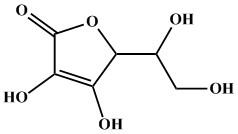
نکته اول: فرمول مولکولی آن C6H8O6 است.
نکته دوم: هر مولکول آن ۶ اتم کربن، ۸ اتم هیدروژن و ۶ اتم اکسیژن دارد.
نکته سوم: نام تجاری آن آسکوربیک اسید است.
نکته چهارم: تعداد اتم های کربن و اکسیژن آن با تعداد اتم های کربن و اکسیژن مولکول گلوکز برابر است.
نکته پنجم: تعداد اتم های هیدروژن آن ۴ تا کمتر از تعداد اتم های هیدروژن مولکول گلوکز است.
نکته ششم: یک ترکیب غیر آروماتیک است.
نکته هفتم: ۴ گروه عاملی هیدروکسیل دارد.
نکته هشتم: یک گروه عاملی استری دارد.
نکته نهم: یک پیوند دوگانه کربن-کربن و یک پیوند دوگانه کربن-اکسیژن دارد. پس در کل دو پیوند دوگانه دارد.
نکته دهم: یک حلقه ۵ تایی دارد که متشکل از ۴ اتم کربن و ۱ اتم اکسیژن است.
نکته یازدهم: یک ترکیب کاملا قطبی است.
نکته دوازدهم: محلول در آب است پس ترکیب آب دوست و چربی گریزی است.
نکته سیزدهم: دارای نیروی بین مولکولی پیوند هیدروژنی است.
نکته چهاردهم: دارای ۴۴ الکترون پیوندی است.
نکته پانزدهم: دارای ۲۲ پیوند کوالانسی است.
نکته شانزدهم: دارای ۲۴ الکترون ناپیوندی است.
نکته هفدهم: دارای ۱۲ جفت الکترون ناپیوندی است.
نکته هجدهم: دارای ۶۸ الکترون در لایه ظرفیت اتم های خود است.
نکته نوزدهم: با رادیکال های فعال واکنش داده و آن ها را پایدار کرده و از واکنش پذیری آنها می کاهد.
نکته بیستم: در شرایط خیلی اسیدی، گروه استری آن امکان شکسته شدن را داشته و دچار واکنش آبکافت استری می شود.
نکته بیست و یکم: پیوند دوگانه آن می تواند با یک مول برم واکنش دهد. بنابراین محلول آب برم را بی رنگ خواهد کرد.
نکته بیست و دوم: جرم مولی آن ۱۷۶ گرم بر مول می باشد و ۴ گرم کمتر از جرم مولی گلوکز می باشد.
نکته بیست و سوم: این ترکیب در مرکبات مثل پرتقال یافت می شود.
نکته بیست و چهارم: فقط الکترون هایی با l = 0 و l = 1 در ساختار آن وجود دارد.
نکته بیست و پنجم: در هسته اتم های آن ۹۲ تا پروتون وجود دارد.
نکته بیست و ششم: به خاطر پیوندهای هیدروژنی بسیار زیاد، دارای نقطه جوش بسیار بالایی است. به همین خاطر به دما حساس بوده و با افزایش دما قبل از اینکه به نقطه جوش برسد دچار تخریب می شود.
نکته بیست و هفتم: گروه های الکلی آن می تواند با عامل های اسیدی ترکیبات دی اسیدی واکنش داده و پلی استر تشکیل دهند.

تدریس خصوصی و گروهی شیمی دهم و یازدهم و دوازدهم در تهران
 Iranian Chemist شیمیدان ایرانی
Iranian Chemist شیمیدان ایرانی



